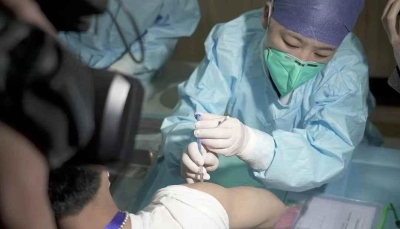
中國新冠疫苗安全嗎?最早“以身試藥”專家回應關切新冠來襲,一場病毒和全人類的“戰爭”爆發。作為抵禦病魔的強有力武器,疫苗被無數人寄予厚望。在這場疫苗研發的攻堅戰中,以國藥集團中國生物技術股份有限公司(下文簡稱中國生物)為代表的中國企業一直走在前列。 新冠疫苗究竟是怎樣研發出來的?從立項獲批到研發、建設、生產、上市,何以只用了330多天時間?究竟應該怎樣看中國生物新冠滅活疫苗的“科研含金量”?中國有近14億人,需要怎樣的覆蓋率……近日,帶著一系列焦點熱點問題,新華每日電訊記者深度對話中國生物董事長、國家“863”計劃疫苗項目首席科學家楊曉明,回應公眾關切。 “以身試藥”是傳統:“9個月時間裏已經被抽了約60管血” 問:《中國疫苗百年紀實》這本書告訴人們,疫苗研發從來不是簡單的事,而是以命相搏。這次新冠疫苗研發也是這樣嗎? 答:是的,我是去年3月23日最早接種我們研發疫苗的人,作為最早一批“以身試藥”者,接種新冠滅活疫苗後沒有任何異常情況,就是打針的地方稍微疼一點。因為接種後要定期檢測抗體,我在9個月時間裏已經被抽了約60管血,因為要定期觀察的血液指標比較多。打第一針後的第二個星期就能檢測到抗體,打第二針後2周左右就能檢測出較高的抗體水平。 一百年來,我國生物製品工作者的獻身精神不斷傳承延續。其中,“以身試藥”就是一個傳統。新冠滅活疫苗臨床試驗中,累計有幾萬名入組受試者接種疫苗,其中很多是生物製品人。這些特殊的志願者,如傳說中的神農嘗百草一樣,用自己的實際行動踐行一名生物製品人的責任與擔當,當然,同時也是基於對我們研發和生產技術的自信。 為助力新冠病毒滅活疫苗早日上市,中國生物在2020年3月底啟動了志願接種,包括國藥集團四級企業黨政主要負責人在內的數十名志願者擼起袖子,自願參加了人體預測試。中國生物人有句話:做敢給自己家人打的疫苗。這是我們的追求,也是我們的自信。 從立項獲批到研發、上市共330多天:“時間前所未有的短” 問:此次中國生物的新冠疫苗從研發到上市用了多久?有哪些關鍵節點? 答:疫苗從立項獲批到研發、上市,總計用了330多天的時間,從科學的角度看,可以說前所未有的短。 中國生物的新冠疫苗從研發到上市,有幾個主要節點:一是2020年4月12日,武漢生物製品研究所研發的新冠滅活疫苗全球首家進入Ⅰ/Ⅱ期臨床試驗,4月27日北京生物製品研究所研發的新冠滅活疫苗也進入Ⅰ/Ⅱ期臨床試驗。 二是2020年6月23日阿聯酋國際臨床試驗,也就是Ⅲ期臨床試驗正式獲批。 三是國內緊急使用,武漢生物製品研究所在2020年6月30日獲得了緊急使用許可,北京生物製品研究所在7月23日獲得許可。 四是國外緊急使用,阿聯酋2020年9月14日首先批準緊急使用,緊接著巴林於11月3日、埃及於2021年1月2日也批準緊急使用。 五是國際上註冊上市,阿聯酋2020年12月9日批準正式註冊上市,巴林12月13日批準正式上市。 六是在國內第一家附條件上市,時間是2020年12月30日。 中國生物的新冠病毒滅活疫苗,從啟動科技攻關到獲批臨床試驗,我們用了98天;從進入臨床到武漢、北京兩個所先後都做完Ⅰ/Ⅱ期臨床試驗,用了78天;再從Ⅲ期臨床試驗入組啟動,到附條件上市獲批,用了168天。 疫苗研發速度很快:“把一天當作幾天用” 問:作為疫苗研發第一梯隊,短時間內拿出疫苗,靠的是什麽? 答:這次中國生物新冠滅活疫苗的研發速度很快,很大程度上得益於舉國體制優勢。 從全球經驗看,過去一種疫苗從研發到上市,一般需要10年以上,投入10個億以上。速度快一些的,也需要5年到6年時間。所以,新冠疫苗330多天能夠上市,我們可以說是一個奇跡。這次新冠滅活疫苗的研發速度之所以能夠這麽快,關鍵在於依靠國家強大的制度優勢。整個疫苗的研發過程得到了國家很多部委的大力支持,包括科技部、衛健委、藥監局、工信部等。各部門採取應急狀態的研發和審批程序,很多技術路線並行開展,各疫苗研發審評機構將審評程序由“串聯”變“並聯”,使得疫苗研發、審批時間最大限度縮短。 同時,中國生物在內部推行了最激烈的競爭。中國生物為新冠疫苗啟動了“背靠背”的科技攻關競賽,直接推動了同一疫苗研發在兩個不同企業之間的進度。武漢生物所和北京生物所承接研發課題後,在同一個賽場的兩條賽道上展開競賽,這個新機制上的改革,最大限度激發了科研人員的競爭動力,也為疫苗研發“雙保險”打下了基礎。 為了提高效率,我們在研發過程中不計投入,採取了許多“串聯”改“並聯”的工作模式。以小鼠的動物試驗來說,為了更快找到合適的註射劑量,我們一改通常的試驗方式,改為三組不同劑量的試驗同時進行。這就需要研究團隊加班加點,把一天當作幾天用。疫苗研發不僅是技術活也是體力活,短時間內拿出疫苗,靠的是研發團隊爭分奪秒的拼搏精神。 中國生物新冠滅活疫苗具有五大特點:“滅活疫苗是個既傳統又現代的技術” 問:在疫苗的諸多技術路線中,中國生物為什麽最終選擇滅活這一技術路線? 答:中國生物新冠滅活疫苗具有技術安全性、防護有效性、人群普適性、儲運便捷性和產能可及性等特點,安全性非常好,有效性數據超過了臨床研究預設的目標,冷鏈儲運條件符合全球大多數國家的國情,產能充足,能夠滿足大範圍的接種使用。 同時,有別於過去的滅活疫苗生產技術,中國生物採用先進的細胞培養技術、純化工藝技術及質量控制方法,生產效率高,質量控制指標完全達到國際先進水平。 截至目前,全球範圍內成功上市的疫苗大部分是滅活疫苗產品,包括脊髓灰質炎疫苗(一類新藥)、手足口病疫苗(一類新藥)、森林腦炎疫苗(一類新藥)、出血熱疫苗等。 新冠滅活疫苗將全病毒進行培養,然後通過滅活和純化,製備成滅活疫苗,其抗原成分完整,保護性更加全面。2020年7月中國生物新冠疫苗獲批緊急使用以來,在自願、知情、同意的前提下,對高風險暴露人群累計完成數百萬劑次的新冠疫苗緊急接種工作。其中7萬多人赴海外一百多個國家有發病的疫區工作,在同一工作生活環境下,接種疫苗者中沒有病例報告。 此外,疫苗的可及性也是非常重要的參考指標。在可及性方面,滅活疫苗有著自己的儲運便捷性優勢,儲運條件是2℃~8℃,這與我國以及許多國家現有的疫苗儲存條件和運輸條件一致,不需要重構冷鏈體系設施,可大規模降低成本。 “對於疫苗的安全性,接種者不用擔心” 問:近期,英國發現的變異新冠病毒備受關注,新冠疫苗對變異後的病毒是否有效? 答:從我們目前收集到的數據看,全球不同地方分離出來的病毒,我們滅活疫苗產生的抗體全部可以覆蓋。 國家藥監局審評通過的分析數據顯示疫苗保護效力為79.34%,高於世界衛生組織50%的指標。一般來說,多數疫苗有效率超過70%即可在我國上市。在呼吸道疾病疫苗普遍保護率相對較低的情況下,我們的新冠疫苗屬於“優等生”。 2020年底,國家藥監局批準中國生物的滅活新冠疫苗附條件上市。“附條件上市”相當於給企業留了“家庭作業”,主要是持續監測觀察抗體的持久性等。對於疫苗的安全性,接種者不用擔心。2021年1月13日,國務院聯防聯控機制發佈會介紹,我國已累計開展重點人群新冠病毒滅活疫苗接種超1000萬劑次,證明新冠病毒滅活疫苗具有良好的安全性。 很多一線研發人員“精神和身體都飽經考驗” 問:在新冠疫苗的研發歷程中,無數一線工作者默默付出,成就了疫苗的快速成功上市,背後有哪些不為人知的感人故事? 答:2020年的大年初一,我們的一位科研人員接到了新冠疫苗研發任務。為投身抗疫一線,她緊急決定留下年僅2歲的女兒,從安徽老家連夜自駕逆行趕回武漢,經過近5個小時的奔波,終於在封城前夜趕到,隨即被派到中國疾病預防控制中心的高等級生物安全實驗室(P3實驗室)開始工作。 因為在實驗室裏要穿非常厚的防護服,穿脫一次很費時間,為了節約時間,我們很多一線研發人員都讓自己盡量少吃東西,少喝水,甚至後來還穿著紙尿褲,凌晨三四點鐘才能脫下防護服,回到休息區,精神和身體都飽經考驗。 中國疫苗找到了國際臨床試驗合作新的“打開方式” 問:此次是中國疫苗首次在海外大規模開展上市前的Ⅲ期臨床試驗,海外臨床試驗情況如何? 答:過去,由於國際化程度不夠高,國內生物制藥企業在海外還沒有開展過大規模的保護性臨床研究。可以說,通過這次磨煉洗禮,中國疫苗找到了國際臨床試驗合作新的“打開方式”。 在海外臨床試驗方面,我們與阿聯酋、巴林、阿根廷、埃及、秘魯等國家開展合作,綜合考慮國家的合作意願和醫療衛生及科研條件,這幾個國家的政府部門都非常支持,一些國家領導人、知名政要都主動成為疫苗接種的志願者。 中國生物新冠疫苗的臨床試驗嚴格採取國際上通行的隨機、雙盲、對照的方式。“雙盲”就是指研究者和疫苗的接種者都不知道每個人打的是安慰劑還是疫苗,安慰劑和疫苗從外觀到註射方式以及後期監測手段都完全一樣,最大限度減少人為因素對試驗結果可能造成的幹擾。 從參與Ⅲ期臨床試驗的人員規模來說,我們在國際上開展了覆蓋志願者國別最多的臨床試驗,Ⅲ期臨床試驗接種人數超過了6萬人,接種志願者涵蓋了125個國籍,覆蓋人群及其所屬國別量均創全球第一。 此外,從中國到海外參與臨床試驗的團隊不僅有國藥集團和中國生物的團隊,還有來自國家疾控中心、河南省疾控中心的專業人員,以及第三方臨床監查方。我們與當地的合作夥伴及一流的研究團隊密切合作,取得了很好的效果。 建立較穩固的群體免疫屏障:理論上“中國要接種的人數範圍在9億至12億” 問:中國有近14億人,需要怎樣的覆蓋率,才能通過註射疫苗構築起免疫之墻和保護屏障? 答:在新冠病毒來襲之前,我國還沒有一個高等級的生物安全生產設施。我們借鑒高等級病原微生物實驗室建設標準和自身生產工藝特點,分別在北京和武漢建成的新冠滅活疫苗高等級生物安全生產車間,經國家有關部門檢查和認證後,已投入規模化生產,今年預計產能可達到10億劑以上。 根據以往疫苗預防接種的效果觀察,結合新冠疫苗臨床試驗顯示的保護率,理論上需要有70%至85%左右的人群接種疫苗,才可能建立較穩固的群體免疫屏障。以此來算,中國要接種的人數範圍在9億至12億人。 新冠疫苗整條生產線:設備實現了95%的國產化率 問:我們的新冠疫苗生產線自主化程度如何? 答:從2020年1月23日武漢封城,到3月23日我接種第一針疫苗,只用了2個月的時間。中國生物能這麽快做出疫苗,並且今年產能將達到10億支,在全世界範圍內看都是很不容易的。 滅活疫苗是傳統、經典的路線,我要特別強調滅活路線它不是“落後”,這次新冠疫苗的誕生,裏面包含了很多的創新因素,包括生產工藝技術的創新和質量標準的提升。同時通過這次車間的建設,創造了車間建設的“火神山”速度,實現了整條生產線設備95%的國產化率。 近年來,有關部門提出加強以企業為主體的科技創新體系建設,支持疫苗、生物技術等相關的科技攻關,使我們在疫苗的研發、創新、產業化以及相關的產業鏈方面都取得了提升和突破,因此才能在這麽短的時間研發出新冠疫苗。 臨床精準診斷的“探照燈”和重癥患者救治的“壓艙石” 問:在構築新冠防線上,除了新冠疫苗,中國生物還有哪些建樹? 答:面對突如其來的新冠肺炎疫情,中國生物迅速研發出新冠病毒核酸分子檢測試劑這個臨床精準診斷的“探照燈”,率先提出康復者恢復期血漿療法這個重癥患者救治的“壓艙石”。 2020年2月1日,中國生物採集到了第一例康復者的血漿,對血漿進行核酸檢測、病毒滅活工藝等工序後,通過成熟的血漿製備技術,研發製備出新冠康復者恢復期病毒滅活血漿,系統提出了康復者恢復期血漿採漿計劃、技術標準和臨床治療方案。康復者血漿治療技術,獲得國務院聯防聯控機制推薦使用,納入國家衛健委《診療方案》,被專家形容為治療的“壓艙石”。 打通產業鏈條,提升核心競爭力:“不是某一個企業的事” 問:我國疫苗或生物製品的研制、生產還存在哪些問題? 答:在國家間相互競爭的時候,卡脖子技術能成為致命因素,這時一定要有一個全產業鏈。產業發展需要全產業鏈的互動,在這方面,中國有著巨大潛力,也需要加大科技創新和資金與人才的投入。 我舉個例子,生物制藥行業遇到過三個門檻,其中之一就是規模化哺乳動物細胞的培養問題。現在生物反應器全自動微載體培養技術已經達到了很高的水平,因此為新冠疫苗的研發奠定了堅實的基礎。 同時也要時刻關注科技創新成果轉化機制。與過往相比,我們的轉化機制已經暢通許多,但在機制的靈活性、整體的協同性上,較之歐美還是存在一定差距,這需要我們進一步改革提升,堅持問題導向、目標導向,打通產業鏈條,提升核心競爭力。這不是某一個企業的事,需要國際國內、國企民企、科研院所、大專院校、政府監管部門等多方面的合作,共同去推動、共同去挑戰、共同去實現。 疫苗安全問題“需要系統全面地規劃” 問:我國不久前通過生物安全法,您如何看待疫苗對國家安全的重要作用? 答:中國生物在全國率先建立了高等級生物安全疫苗生產管理體系,配合相關部門編制了首個疫苗生物安全生產設施標準,並為國家制定《疫苗生產車間生物安全通用要求》提供了藍本。這是我們在疫苗研發之外的另一條戰線,它不光關系到我們之前贏得的疫苗研發的速度優勢能不能迅速轉化為生產能力,還關系到今後突發重大傳染病疫情時的疫苗研發生產效率,關系到國家生物安全戰略實施,關系到我國在全球生物科技競爭中能不能處於有利地位。 當然,疫苗安全不僅僅是疫苗企業自己的事,需要系統全面地規劃。建議:一是繼續著力固根本、強弱項、補短板,加強疫苗研發能力建設,政府、科研院所支持國家疫苗發展戰略,鼓勵科技創新和產業合作。 二是有序引導,加強資源統籌,逐步改變小而散的疫苗行業局面,確保在任何特殊時期都能始終牢牢把握疫苗供應保障主動權。 三是加強工業能力提升,涉及疫苗相關上下遊產業鏈的裝備制造水平、原輔材料供應能力,要在國家主導下,有計劃地實施專項提升。 四是加強疫苗專業人才培養,通過政策引導和扶持,培育和打造行業領軍人物和企業科研“靈魂”,培養造就一大批專業技術人才、能工巧匠。 五是註重生物安全實驗室及生產設施的佈局規劃,鼓勵企業打好生物安全硬件和軟件建設基礎,為應對突發新發傳染病做好準備。 |